脂质体是近几十年来被研究开发广泛的纳米给药系统,其可实现对多种药物活性成分的包载而广受研究者们的欢迎。而目前,也已经有多达15个脂质体处方在临床上得以使用,越来越多的脂质体相关研究项目也逐渐涌现。然而,由于脂质体自身性质以及功能方面的特殊性,其制备过程也较之传统制剂复杂许多,所以业内常将脂质体类制剂称为“复杂注射剂”。目前,主要的脂质体制备方法包括:薄膜水化法、反向蒸发法、乙醇注入法、乙醚注入法等,以及新的技术微流控法制备脂质体。本文中,我们就将通过近期的相关研究对比传统的薄膜水化法与微流控法在脂质体制备方面的性能差异。
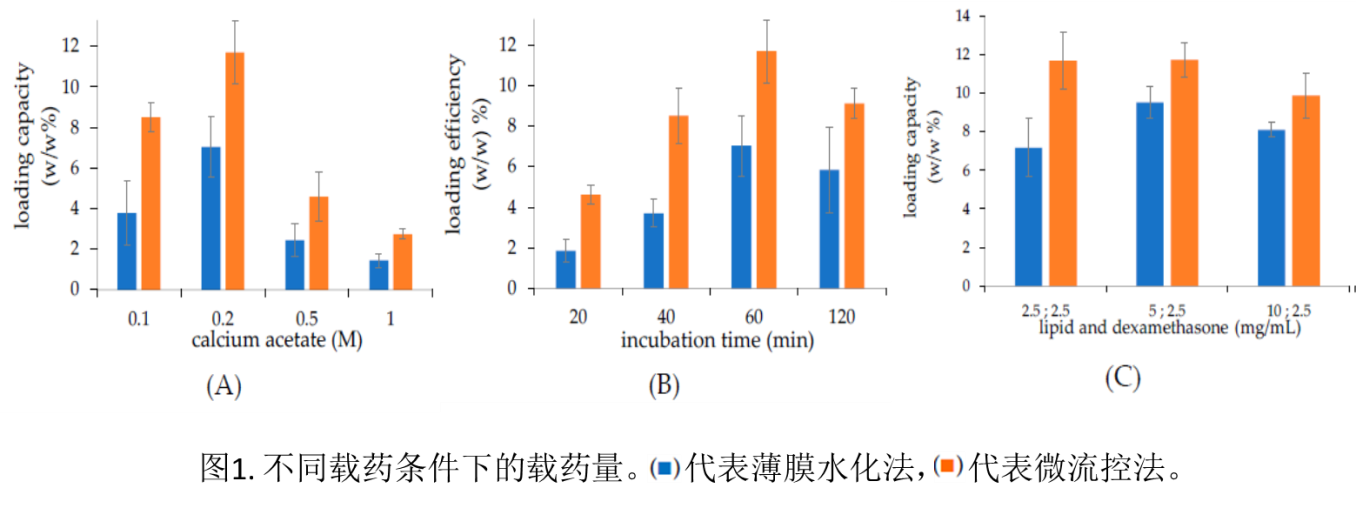
首先,采用地塞米松作为模型药物,地塞米松是一种水溶性药物,并可通过乙酸钙梯度进行主动载药。研究中首先分别通过薄膜水化法与微流控法制得的脂质体,在乙酸钙梯度下进行主动载药,并考察载药量上的差异,结果如图1。可看到,在不同的载药条件下微流控法相较于薄膜水化法,均有高的载药量。
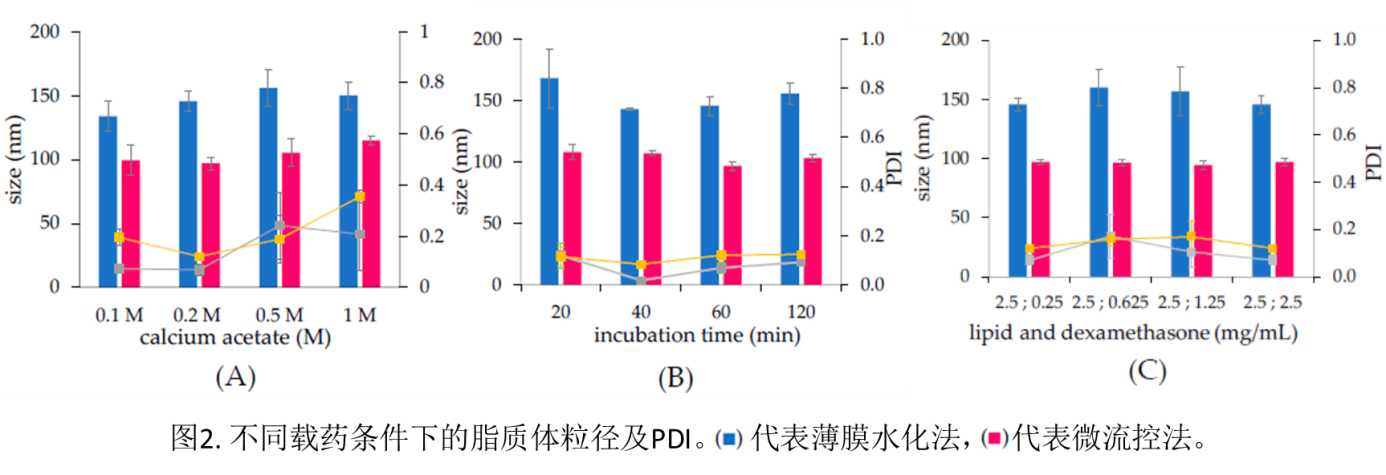
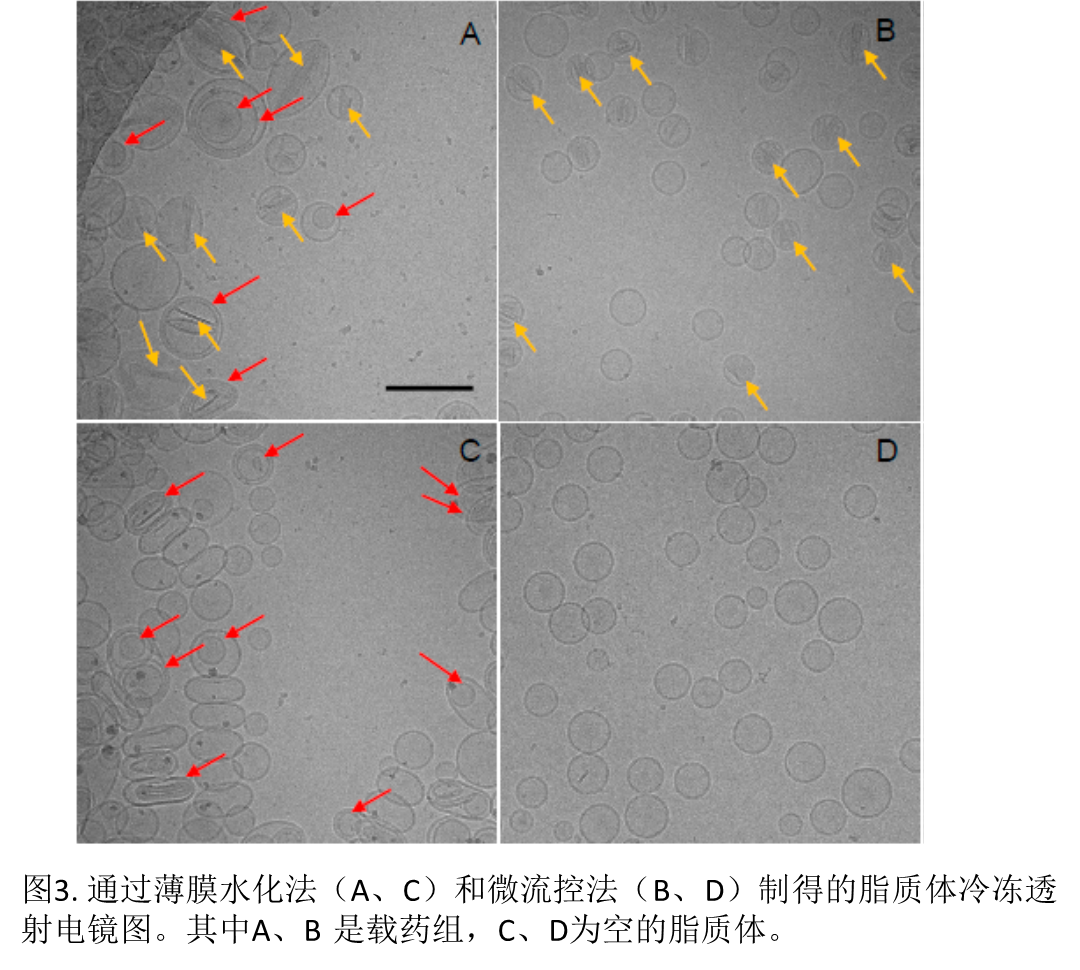
随后,对两种方法制备得到的脂质体分别进行粒径、PDI、形态等的表征。图2中可以看出,微流控法在不同的载药条件下均可以制备得到粒径小的脂质体,而两种方法制得的脂质体的分散性相近(PDI结果接近)。这表明了微流控法在制备脂质体方面有更好的控制效果,可以实现更小粒径的脂质体的制备。并用冷冻透射电镜进行了脂质体的形态学考察,结果如图3所示。可以看到,薄膜水化法制备的脂质体在电镜下大小不一,同时还有很多多层膜结构的脂质体存在,而微流控法制备的脂质体在电镜下呈现出均一的单层膜球形结构,形态更好。
从以上的结果可以看出,相较于传统的薄膜水化法制备的脂质体,微流控方法制备的脂质体可以实现高载药量,并且可更好的实现对粒子的粒径控制与调控,制备得到更小的粒子,而且微流控法制备的脂质体在电镜下观察到了更好的形态与粒子质量。
除此之外,微流控法制备的脂质体在重复性方面表现良好,并且操作更加简易,可以更好的实现生产的放大,这些优势都使得微流控这一新技术在纳米颗粒制备方面愈发受到研究者们的青睐。
参考文献:
[1] Bulbake, U.;Doppalapudi, S.; Kommineni, N.; Khan, W.J.P. Liposomal formulations in clinicaluse: An updated review. Pharmaceutics 2017, 9, 12.
[2] MD Al-Amin.; FedericaBellato.; Francesca Mastrotto. Dexamethasone Loaded Liposomes by Thin-Film Hydrationand Microfluidic Procedures: Formulation Challenges. Int. J. Mol. Sci. 2020,21, 1611.
[3] Dua, J.; Rana, A.;Bhandari, A. Liposome: Methods of preparation and applications. Int. J. Pharm.Stud. Res. 2012, 3, 14–20.
纳米药物制造系统家族

应用范围
-8e7f7151-3392-46f6-ae2a-88cb3f7457c1.png)
随着纳米技术的不断发展,纳米药物在医药领域的应用越来越广泛,尤其在基因治疗,肿瘤靶向等方面显现了优势。锘海生物科学为科研工作者和企业提供纳米药物制备、生产及检测服务,囊括了纳米药物研发过程中,从处方筛选到制剂表征的全线过程。为客户简化流程,节约时间成本,同时提供高质量的数据分析与技术支持服务。
技术服务方案选择
方案一:客户确定载体和药物活性成分API以及已有的protocol,锘海提供纳米制剂制备,包括粒径和包封率检测。
方案二:针对科研客户,课题中纳米制剂设备相关部分可完全外包,根据客户选择的载体和API,确定处方并制备纳米制剂,最后提供检测报告和protocol。
方案三:针对企业客户,提供从载体选择到纳米制剂制备全线服务,即完整R&D过程。
方案四:提供仪器样机进行租赁,并对客户进行培训及技术支持,帮助客户完成制剂研发。
选择我们的理由
科研:好的制备方法 · 稳定的结果 · 完整的protocol · 详细的分析报告 · 更短的测试周期。
企业:从R&D到生产(cGMP)无缝放大的方案 · 严格的SOP · 低研发成本 · 短项目周期 · 遵守客户资料保密原则。






-8e7f7151-3392-46f6-ae2a-88cb3f7457c1.png)